醫療設備CE-MDR認證標簽上應注明哪些信息?
醫療設備CE認證標簽上應注明哪些信息?
《醫療器械法規》(MDR)不久將適用,并將要求在醫療器械標簽上注明各種信息。制造商如何在短期內以協調的方式遵守這些要求?
歐洲擁有24種官方語言,因此必須使用符號來傳達標簽上的所需信息。MDR的附件I第三章23.2規定了標簽必須包含哪些信息,從簡單的“醫療設備”到UDI承運人。MDR允許在標簽上使用符號代替書面語言(附件I,第三章,23.1.h)。
信息量很大,可以減輕制造商的工作負擔MedTech Europe已發布了符號設計,標題和翻譯,并建議在國際上使用它們。但是,必須在與MDR 23.1.H一致的使用說明書中對其進行描述,直到未在統一標準中發布它們為止。
如果特殊情況需要,鼓勵制造商使用以下符號,始終以如下所示的順序使用 -旨在加快用戶對符號及其含義的認識和接受。
歐洲醫療技術提議的符號設計:
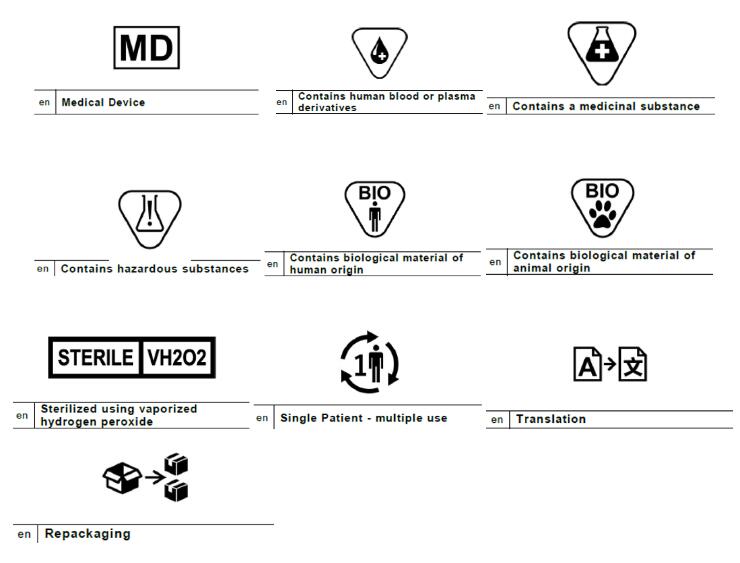
此外,作為文本的替代,還建議在植入卡上使用以下符號(MDR第18條):










